拞榓斀墳
俙丂巁丒墫婎偺拞榓
拞榓斀墳丗巁偲墫婎偐傜墫偲悈傪惗偠傞斀墳丄傑偨偼巁偐傜惗偠傞悈慺僀僆儞俫+偲丄
丂丂丂丂丂丂丂墫婎偐傜惗偠傞悈巁壔暔僀僆儞俷俫-偐傜丄悈俫2俷偑惗偠傞斀墳丅
亙椺亜
俫2俽俷4亄俀俶倎俷俫仺俶倎2俽俷4亄俀俫2俷
墫丗巁偺堿僀僆儞偲墫婎偺梲僀僆儞偐傜側傞壔崌暔丅
俛丂拞榓揔掕
拞榓揔掕丗拞榓斀墳傪棙梡偟偰丄擹搙偺傢偐偭偰偄側偄巁乮傑偨偼墫婎乯偺悈梟塼偺
丂丂丂丂丂丂丂擹搙傪媮傔傞憖嶌丅
亙椺亜
俫2俽俷4亄俀俶倎俷俫仺俶倎2俽俷4亄俀俫2俷
丂侾mol丂丂丂丂俀mol丂丂丂丂侾mol丂丂丂 俀mol
巁偲墫婎偑偪傚偆偳拞榓偡傞偲偒丄師偺娭學偑惉傝棫偮丅
乮巁偺壙悢乯亊乮巁偺暔幙検乯亖乮墫婎偺壙悢乯亊乮墫婎偺暔幙検乯
偙偺幃偼丄師偺傛偆偵彂偒姺偊傜傟傞丅
乮巁偺壙悢乯亊乮巁偺儌儖擹搙[mol/l]乯亊乮乮巁偺懱愊[cm3]乯/1000乯
亖乮墫婎偺壙悢乯亊乮墫婎偺儌儖擹搙[mol/l]乯亊乮乮墫婎偺懱愊[cm3]/1000乯
揔掕幚尡婍嬶
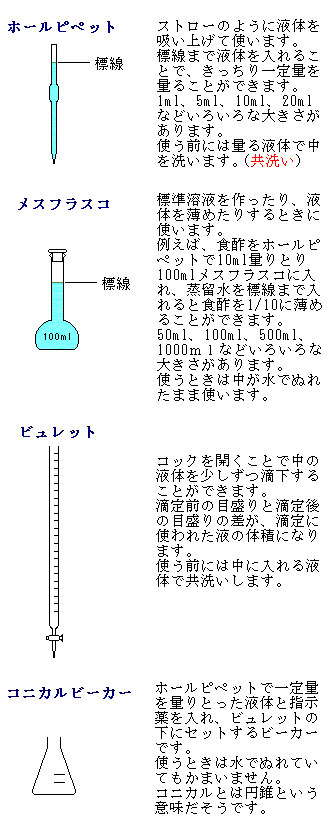
偒偭偐傝懱愊傪検傞儊僗僼儔僗僐丄儂乕儖僺儁僢僩丄價儏儗僢僩偼壛擬姡憞偟偰偼偄偗側偄丅
乮僈儔僗偑擬偱朿挘偟偰偟傑偆乯
怘恷偲悈巁壔僫僩儕僂儉悈梟塼偺拞榓揌掕
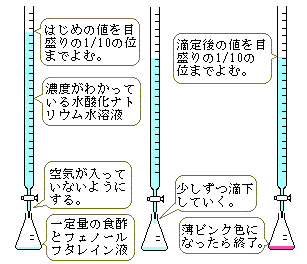
俠丂揔掕嬋慄
揔掕嬋慄丗拞榓斀墳偺嵺丄壛偊偨巁丒墫婎偺懱愊偲崿崌梟塼偺倫俫偺娭學傪昞偟偨
丂丂丂丂丂丂丂僌儔僼丅拞榓揰晅嬤偱傎傏悅捈乮倫俫偑戝偒偔曄壔乯偵側傞丅
偁偲偼嫵壢彂尒偰倵
俢丂拞榓揰偺塼惈
拞榓揰偱偺梟塼偺塼惈偼丄昁偢偟傕乽拞惈乿偱偁傞偲偼尷傜側偄丅
拞榓揰偱偼乽墫亄悈乿丅備偊偵丄埲壓偺偙偲偑偄偊傞丅
丒嫮巁亄嫮墫婎佀拞惈
丒嫮巁亄庛墫婎佀巁惈
丒庛巁亄嫮墫婎佀墫婎惈
仠墫偺庬椶
丒惓墫丗墫偺拞偵丄俫偲俷俫偑巆偭偰偄側偄傕偺丅
丂丂丂俶倎俠倢丄俠俫3俠俷俷俶倎丂側偳
丒巁惈墫丗墫偺拞偵丄俫偑巆偭偰偄傞傕偺丅
丂丂丂俶倎俫俠俷3丄俲俫俽俷4丄俶倎俫2俹俷4丂側偳
丒墫婎惈墫丗墫偺拞偵丄俷俫偑巆偭偰偄傞傕偺丅
丂丂丂俵倗乮俷俫乯俠倢丄俠倳乮俷俫乯俶俷3丂側偳
拞榓斀墳丗巁偲墫婎偐傜墫偲悈傪惗偠傞斀墳丄傑偨偼巁偐傜惗偠傞悈慺僀僆儞俫+偲丄
丂丂丂丂丂丂丂墫婎偐傜惗偠傞悈巁壔暔僀僆儞俷俫-偐傜丄悈俫2俷偑惗偠傞斀墳丅
亙椺亜
俫2俽俷4亄俀俶倎俷俫仺俶倎2俽俷4亄俀俫2俷
墫丗巁偺堿僀僆儞偲墫婎偺梲僀僆儞偐傜側傞壔崌暔丅
俛丂
拞榓揔掕丗拞榓斀墳傪棙梡偟偰丄擹搙偺傢偐偭偰偄側偄巁乮傑偨偼墫婎乯偺悈梟塼偺
丂丂丂丂丂丂丂擹搙傪媮傔傞憖嶌丅
亙椺亜
俫2俽俷4亄俀俶倎俷俫仺俶倎2俽俷4亄俀俫2俷
丂侾mol丂丂丂丂俀mol丂丂丂丂侾mol丂丂丂 俀mol
巁偲墫婎偑偪傚偆偳拞榓偡傞偲偒丄師偺娭學偑惉傝棫偮丅
乮巁偺壙悢乯亊乮巁偺暔幙検乯亖乮墫婎偺壙悢乯亊乮墫婎偺暔幙検乯
偙偺幃偼丄師偺傛偆偵彂偒姺偊傜傟傞丅
乮巁偺壙悢乯亊乮巁偺儌儖擹搙[mol/l]乯亊乮乮巁偺懱愊[cm3]乯/1000乯
亖乮墫婎偺壙悢乯亊乮墫婎偺儌儖擹搙[mol/l]乯亊乮乮墫婎偺懱愊[cm3]/1000乯
揔掕幚尡婍嬶

偒偭偐傝懱愊傪検傞儊僗僼儔僗僐丄儂乕儖僺儁僢僩丄價儏儗僢僩偼壛擬姡憞偟偰偼偄偗側偄丅
乮僈儔僗偑擬偱朿挘偟偰偟傑偆乯
怘恷偲悈巁壔僫僩儕僂儉悈梟塼偺拞榓揌掕

俠丂
揔掕嬋慄丗拞榓斀墳偺嵺丄壛偊偨巁丒墫婎偺懱愊偲崿崌梟塼偺倫俫偺娭學傪昞偟偨
丂丂丂丂丂丂丂僌儔僼丅拞榓揰晅嬤偱傎傏悅捈乮倫俫偑戝偒偔曄壔乯偵側傞丅
偁偲偼嫵壢彂尒偰倵
俢丂
拞榓揰偱偺梟塼偺塼惈偼丄昁偢偟傕乽拞惈乿偱偁傞偲偼尷傜側偄丅
拞榓揰偱偼乽墫亄悈乿丅備偊偵丄埲壓偺偙偲偑偄偊傞丅
丒嫮巁亄嫮墫婎佀拞惈
丒嫮巁亄庛墫婎佀巁惈
丒庛巁亄嫮墫婎佀墫婎惈
仠墫偺庬椶
丒惓墫丗墫偺拞偵丄俫偲俷俫偑巆偭偰偄側偄傕偺丅
丂丂丂俶倎俠倢丄俠俫3俠俷俷俶倎丂側偳
丒巁惈墫丗墫偺拞偵丄俫偑巆偭偰偄傞傕偺丅
丂丂丂俶倎俫俠俷3丄俲俫俽俷4丄俶倎俫2俹俷4丂側偳
丒墫婎惈墫丗墫偺拞偵丄俷俫偑巆偭偰偄傞傕偺丅
丂丂丂俵倗乮俷俫乯俠倢丄俠倳乮俷俫乯俶俷3丂側偳
br仺
main_box